Was wird in Kiel geforscht?
Die Evolution von Antibiotikaresistenzen steht im Mittelpunkt einer globalen Gesundheitskrise. In Kiel beschäftigen sich Forschende damit, wie gezielte Kombinationen von Antibiotika die Resistenzen umgehen oder sogar ausnutzen können. Mit den Erkenntnissen der Evolution entwickeln und testen sie neue Behandlungsprotokolle.
Evolutionäre Ansätze in der Antibiotikaforschung

Neue Behandlungsmethoden mit den verfügbaren Antibiotika können eine vielversprechende Alternative zu herkömmlichen Therapien darstellen. Dabei wird die Evolution der Resistenzen und der Bakterien untersucht. Mit diesem Thema beschäftigen sich Forschende in der Arbeitsgruppe von Professor Hinrich Schulenburg an der Christian-Albrechts-Universität in Kiel. Zum Beispiel in Evolutionsexperimenten untersuchen die Forschenden, wie sich Bakterien unter unterschiedlichen Bedingungen verhalten.
Viele Antibiotikabehandlungen setzen nur ein einziges Antibiotikum ein. Dies wird als Monotherapie bezeichnet. Eine Alternative ist es, Antibiotika zu kombinieren. In dieser Kombinationstherapie können zwei oder mehr Antibiotika entweder gleichzeitig oder in zeitlicher Variation verabreicht werden. Letzteres wird als sequentielle Therapie bezeichnet. Für Bakterien-Populationen stellt eine schnelle Veränderung der Umgebung eine große Herausforderung dar, denn durch die Wechsel der Antibiotika wirken in kürzester Zeit unterschiedliche Selektionsdrücke. Unter diesen wechselnden Bedingungen können sich Organismen schlechter anpassen.
Dieser Ansatz kann optimiert werden, indem Antibiotika verwendet werden, die auf unterschiedliche Weise auf die bakterielle Zelle wirken. Dabei werden gezielt evolutionäre Trade-Offs oder induzierte physiologische Veränderungen ausgenutzt. Dieser Ansatz der sequentiellen Therapie wird bisher so gut wie gar nicht in der Medizin eingesetzt, gleichzeitig aber durch Ergebnisse aus der evolutionsmedizinischen Grundlagenforschung als vorteilhaft angesehen.
Schnelle Wechsel von Antibiotika
SICK
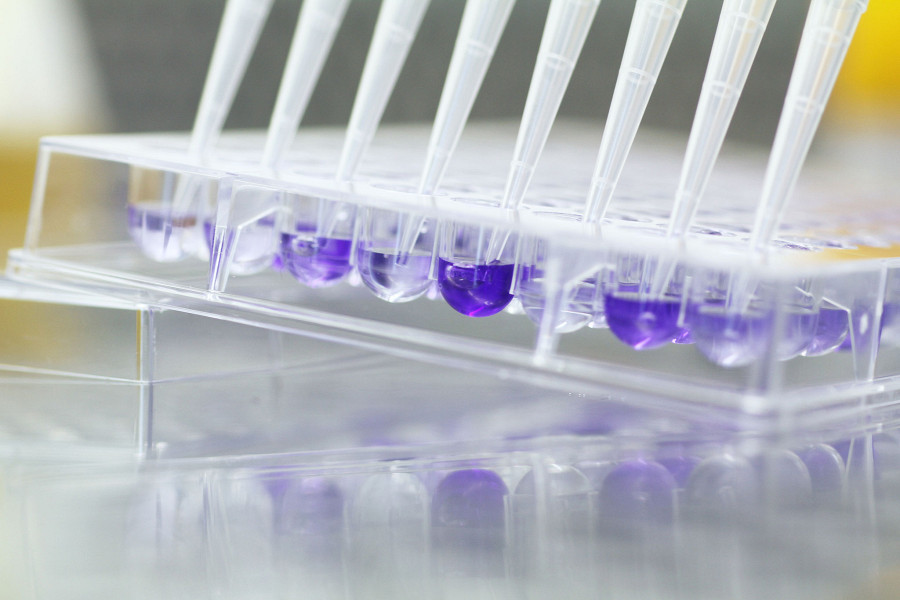
Das Experiment zeigt die Ausbreitung von Resistenzen in einer Bakterienpopulation und verdeutlicht, dass geringe Konzentrationen von Antibiotika (z.B. im Abwasser) den Bakterien helfen Resistenzen aufzubauen. Je mehr Mutationen Bakterien nacheinander durchlaufen, desto stärkere Resistenzen können sie ausbilden. Hätten die Forschenden die Konzentration des Antibiotikums in der zweiten Phase direkt auf die 1000-fache Konzentration erhöht, hätten die Bakterien nicht überlebt.
MultiResi Postkarte Sick
good to know
Bakterien tragen DNA nicht nur auf ihrem Chromosom, sondern auch auf Plasmiden. Das sind kleine Ringe aus doppelsträngiger DNA, die zum Beispiel Gene tragen, um die Wirkung von Antibiotika zu verhindern. Solche Resistenzplasmide können leicht an andere Bakterien weitergegeben werden. Zwei Bakterien bauen einen Kontakt über ihre Zellwände auf, sodass ein kleiner Durchgang entsteht. Das Plasmid wird verdoppelt, während eine Kopie des Plasmids durch den Durchgang zum zweiten Bakterium geschoben wird. Am Ende ist das Plasmid in beiden Bakterien vorhanden und die Bakterien trennen sich wieder voneinander.

Evolutionäre Trade-Offs nutzen
Wenn Bakterien mit Antibiotika behandelt werden, wirkt ein Selektionsdruck auf sie. Das begünstigt die Überlebenschancen von Bakterien, die bereits eine Resistenz gegen das Antibiotikum aufweisen. Die Entwicklung und Aktivierung einer Resistenz kann jedoch Nachteile mit sich bringen. Im einfachsten Fall bedeutet dies, dass resistente Bakterien unter normalen Bedingungen ohne Antibiotika schlechter wachsen können, weil die Resistenz Energieaufwand erfordert. Dies nennt man einen evolutionären Trade-off, also eine Kompromissbildung, die aufgrund der Entwicklung einer neuen Eigenschaft entsteht. Ein besonderer Fall eines solchen evolutionären Trade-offs tritt auf, wenn eine Resistenz gegen ein bestimmtes Antibiotikum dazu führt, dass die Bakterien gleichzeitig empfindlicher gegenüber einem anderen Antibiotikum werden. Dieser Fall wird als evolvierte kollaterale Sensitivität bezeichnet. Das kann in der Behandlung ausgenutzt werden, indem man zwischen den relevanten Antibiotika wechselt, um die empfindlicheren Bakterien abzutöten.
Neben Mutationen im Genom können auch physiologische Veränderungen ausgenutzt werden. Das sind keine Veränderungen der DNA, sondern zum Beispiel Aktivitätsveränderungen bestimmter Stoffwechselprozesse in den Bakterien. Der Kontakt mit einem Antibiotikum kann solche physiologischen Veränderungen auslösen. Diese induzierten physiologischen Veränderungen können dann dazu führen, dass ein weiteres Antibiotikum besser wirkt, z.B. wenn die induzierten Veränderungen die Bakterienzellwand durchlässiger für das Antibiotikum machen. Dieses Phänomen wird als negative Hysterese bezeichnet und ist langanhaltend, jedoch nicht genetisch manifestiert.
Physiologische Veränderungen herbeiführen

Die passende Kombination finden
Die beschriebenen Effekte treten nicht für alle Kombinationen von Antibiotika auf. Die Resistenz gegen ein erstes Antibiotikum kann auch dazu führen, dass Resistenzen gegen weitere Antibiotika auftreten. Sogenannte Multiresistenzen treten häufig gegen Antibiotika mit ähnlichen Wirkmechanismen auf. Hypothesen zu geeigneten Kombinationen werden daher auf Grundlage der unterschiedlichen Wirkmechanismen aufgestellt. Experimentell müssen veränderte Resistenzen bzw. Sensitivitäten überprüft werden. Für die klinische Anwendung ist dabei wichtig, die bereits vorliegenden Resistenzen der Bakterien-Population zu kennen.